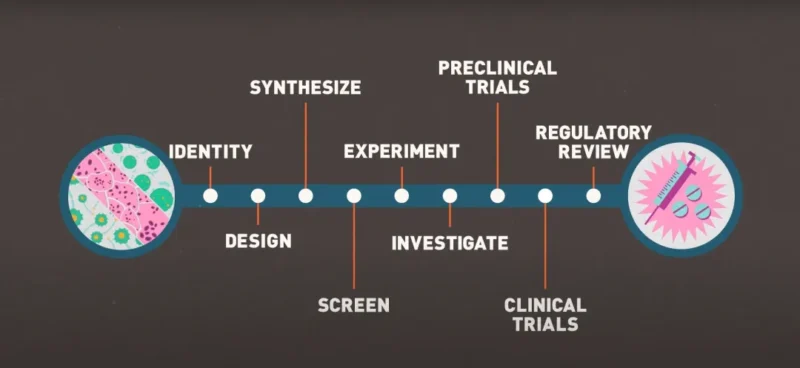
所有在医院进行的试验必须经过国家药监局的批准,拿到临床试验批件或试验通知书后,才能在具备资质的药物临床试验机构申请试验立项
试验进行前还需获得医院伦理委员会的批准,试验方案在获得伦理委员会同意后方可执行。
伦理委员会的职责是保护受试者的权益和安全,应当特别关注弱势受试者
伦理委员会审查是否存在受试者被强迫、利诱等不正当的影响而参加临床试验
那么志愿者如何报名参加临床试验?
第一步
志愿者需要对临床试验基本信息做一个基本了解。可以通过国家药监局官方网站或各大医疗机构网站查询临床试验的信息,初步确定自己是否适合入组某个试验。
第二步
签署知情同意书。知情同意过程遵循“充分告知,完全自愿”的原则
研究者会向受试者或患者告知的内容包括但不限于:
- 临床试验概况
- 试验目的
- 试验治疗和随机分配至各组的可能性
- 受试者需要遵守的试验步骤,包括创伤性医疗操作、受试者的义务、试验预期的获益,以及不能获益的可能性
- 其他可选的药物和治疗方法,及其重要的潜在获益和风险
- 受试者发生与试验相关的损害时,可获得补偿以及治疗
- 受试者参加临床试验可能获得的补偿
- 受试者参加临床试验预期的花费
受试者参加试验是自愿的,可以拒绝参加或者有权在试验任何阶段随时退出试验而不会遭到歧视或者报复,其医疗待遇与权益不会受到影响。
知情同意过程应当以书面的、签署姓名和日期的知情同意书作为文件证明,受试者或患者及研究者各保留一份。
第三步
按照试验的要求完成各项检查和随访。
总之,参加临床试验过程中,患者的权益会得到充分的保障。即使患者参加临床研究并且入组了,也可以随时无条件退组。
以上内容引自:山东大学第二医院-临床试验小知识